Os pacientes com Parkinson que tomam a Levodopa ou L-Dopa, podem estar de alguma forma, desapontados com esse fármaco.
Usado no tratamento das síndromes parkinsonianas, a L-Dopa no primeiro momento, mantém sob controle os tremores e a falta de equilíbrio. Após essa fase de “lua de mel”, com o passar do tempo, a droga vai tornando-se menos eficaz.
Caso os pacientes passem a tomar doses mais elevadas, tem sido constatado que alguns deles começam a ficar em um estado de paralisia, quase num estado de “congelamento”.
A inovação
O Parkinson ocorre quando os neurônios produtores de dopamina no cérebro começam a morrer.
Essa doença ainda não é bem compreendida, mas a razão pela qual a L-Dopa perde a eficácia é conhecida.
Isso acontece porque o cérebro também começa a perder uma enzima conhecida como descarboxilase dos L-aminoácidos aromáticos, ou AADC, que é necessária para converter a L-Dopa em dopamina.
O MIT Technology Review divulgou essa semana que uma empresa de biotecnologia, a Voyager Therapeutics, quer prolongar os efeitos da L-Dopa, utilizando uma abordagem inovadora: a terapia gênica.
A empresa, com sede em Cambridge, Massachusetts, está testando a ideia em pacientes com Parkinson que concordaram em submeter-se a uma cirurgia cerebral e a uma injeção de DNA.

Ator Michael J. Fox, que tem Parkinson, cuja fundação ajudou a custear o desenvolvimento do tratamento experimental da Voyager. (Cortesia: Emmys)
A estratégia da Voyager – que começou testando em pacientes em um estudo mais restrito – é injetar vírus que transportem o gene para a AADC no cérebro. Essa abordagem “volta o relógio“, de modo que a L-Dopa começa a funcionar novamente em pacientes com sintomas avançados, como naquele período da “lua de mel”.
Se você assistir aos vídeos de pacientes que mostram o antes e o depois de tomarem a L-Dopa, fica óbvio porque eles possivelmente vão optar por esse fármaco em uma dose mais baixa. No estado “off”, eles se movimentam em câmera lenta. No estado “on”, quando o fármaco está em ação, alguns ainda ficam trêmulos.
Eles [Os pacientes] ficam bem no início, mas, em seguida, respondem de forma muito irregular à L-Dopa. Este novo ensaio é para restaurarmos a enzima e permitir que os pacientes fiquem mais “despertos”, ou fiquem em estado “on” por um longo período de tempo.” Krystof Bankiewicz, cientista da Universidade da Califórnia e co-fundador da Voyager.

Krystof Bankiewicz, co-fundador da Voyager Therapeutics, começou a usar a terapia genética para o Parkinson há 30 anos. (Crédito: MIT)
A Voyager
A Voyager foi criada em 2013 e faz parte da onda de empresas de biotecnologia que conseguiram captar recursos financeiros para a terapia genética, uma tecnologia que começa a dar frutos: depois de três décadas de pesquisa, alguns produtos estão chegando ao mercado.
Ao contrário dos estudos com drogas convencionais, as que envolvem a terapia genética muitas vezes geram altas expectativas de que o tratamento será bem sucedido. Isso porque a terapia corrige erros de DNA que levam a consequências biológicas conhecidas com exatidão.
“Estamos trabalhando há 60 anos com a farmacologia da dopamina”, diz Steven Paul, CEO da Voyager, e ex-executivo da gigante farmacêutica Eli Lilly. “Se conseguirmos que o gene vá para o tecido certo, no momento certo, seria surpreendente se ele não funcionasse.”
A evolução dos estudos
O conceito de terapia genética voltada para o Parkinson iniciou em 1986, quando Bankiewicz determinou pela primeira que pouca AADC seria a razão da L-Dopa deixar de funcionar. Ele imaginou que a terapia genética pudesse ser uma maneira de corrigir isso. Passou 20 anos para que ele pudesse testar a ideia em 10 pacientes, em um estudo realizado na UCSF.
Nesse teste, Bankiewicz viu que a entrega do gene não teve o sucesso esperado. Poucas células cerebrais foram atualizadas com a nova informação genética, a qual foi transportada para elas por meio de vírus injetados no cérebro. Os pacientes pareciam melhorar, mas não tanto.
Mesmo o tratamento não tendo funcionado como planejado, esse estudo inicial deu destaque a uma abordagem que a Voyager tem utilizado. É possível taguear a AADC com um marcador químico, para que os médicos possam vê-la agindo no cérebro dos pacientes.
Por exemplo, em pacientes da UCSF, a produção contínua da enzima produtora de dopamina ainda é visível no cérebro deles, mesmo vários anos depois.
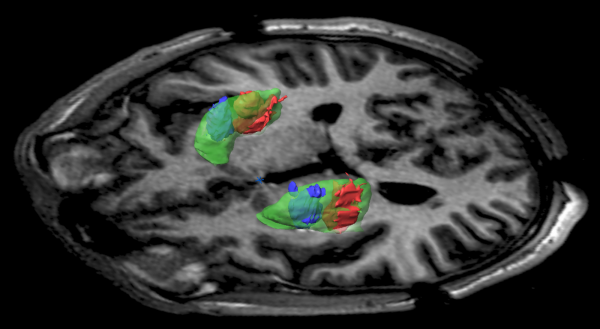
É possível taguear a AADC com um marcador químico, para que os médicos possam vê-la trabalhando no cérebro dos pacientes. (Crédito: MIT)
Por outro lado, em alguns estudos anteriores de terapia genética, os médicos tiveram que esperar até os pacientes morrerem para descobrir se o tratamento tinha sido entregue corretamente. “Anatomicamente, este tratamento nos diz se o levamos para o lugar certo”, disse Paul na matéria do MIT
Esse novo teste está sendo realizado pela Voyager, e foi projetado para levar níveis mais elevados de DNA para os cérebros dos pacientes. O intuito é alcançar melhores resultados.
Para conseguir isso, Bankiewicz desenvolveu um sistema que injeta as partículas virais carregadas de genes através de tubos pressurizados, quando o paciente está dentro de um scanner de ressonância magnética. Dessa forma, o cirurgião pode ver o putâmen, que é a região do cérebro onde o DNA deve chegar e checar se o tratamento foi completo.
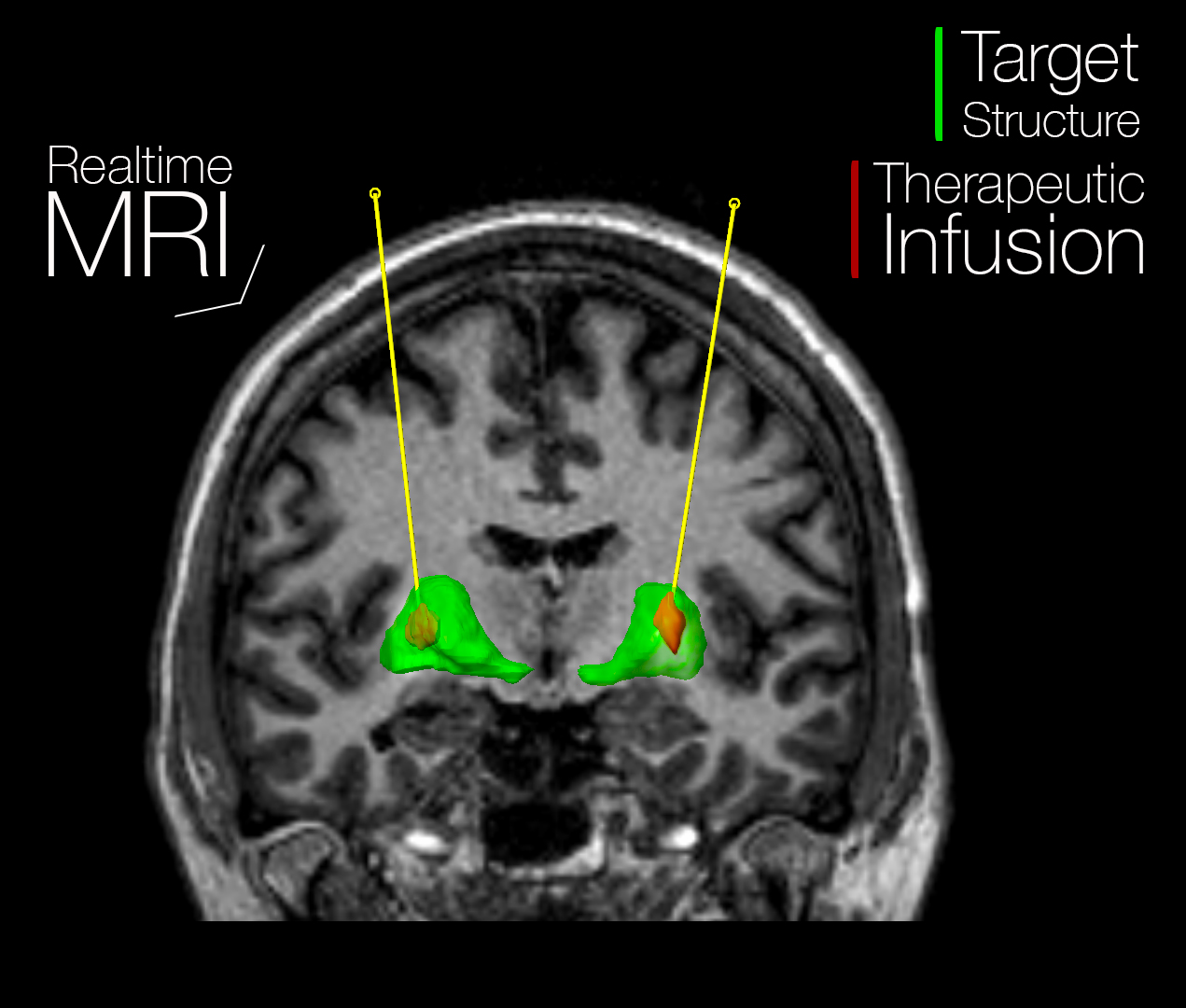
Crédito: Universidade da Califórnia, São Francisco – UCSF
Outros testes
Há outras terapias genéticas para o Parkinson em fase de planejamento ou já em testes. Ao todo, neste ano, houve 48 ensaios clínicos em andamento com substituição de genes ou células no cérebro e no sistema nervoso, de acordo com a Alliance for Regenerative Medicine.
Um estudo desenvolvido na National Institutes of Health busca adicionar um fator de crescimento e regenerar as células. A empresa européia, Oxford BioMedica, está tentando substituir a dopamina.
Segundo o MIT, a equipe da Voyager está entusiasmada em relação a um participante do estudo que eles chamam de “paciente número 6“. Eles vem acompanhando esse paciente por vários meses, desde que ele recebeu o tratamento.
Antes da terapia genética, o “paciente 6” estava tomando uma alta dose de L-Dopa e, mesmo assim, passava seis horas por dia em um estado “desligado”. Agora ele fica nesse estado apenas duas horas por dia e toma menos medicamento.
Este paciente foi o que recebeu a dose mais alta de DNA até o momento, cobrindo a maior área do cérebro. É, em parte por isso, que a Voyager acredita que doses mais elevadas devem mostrar-se mais eficazes.
Eu acredito que o fracasso anterior dos ensaios com terapia genética para o Parkinson foi resultado de uma entrega deficiente”. Krystof Bankiewicz



