Cientistas norte-americanos acabam de criar os primeiros robôs vivos. Os “xenobots”, como são chamados, conseguem se mover, segurar algo (como por exemplo um medicamento que precisa ser transportado para um local específico dentro do corpo de um paciente) e até se autocurar, caso sejam, por exemplo, cortados.
Com menos de um milímetro de comprimento, os “xenobots” foram adaptados de células vivas de embriões de sapos – células estas que foram aglutinadas em formas de vida inteiramente novas.
“São máquinas vivas, uma forma de vida completamente nova”, afirmou Joshua Bongard, que co-liderou essa pesquisa e que também é especialista em robótica na Universidade de Vermont (UVM). “Eles não são um robô destes tradicionais e nem uma espécie de animal. É uma nova classe de artefato: um organismo vivo e programável”.
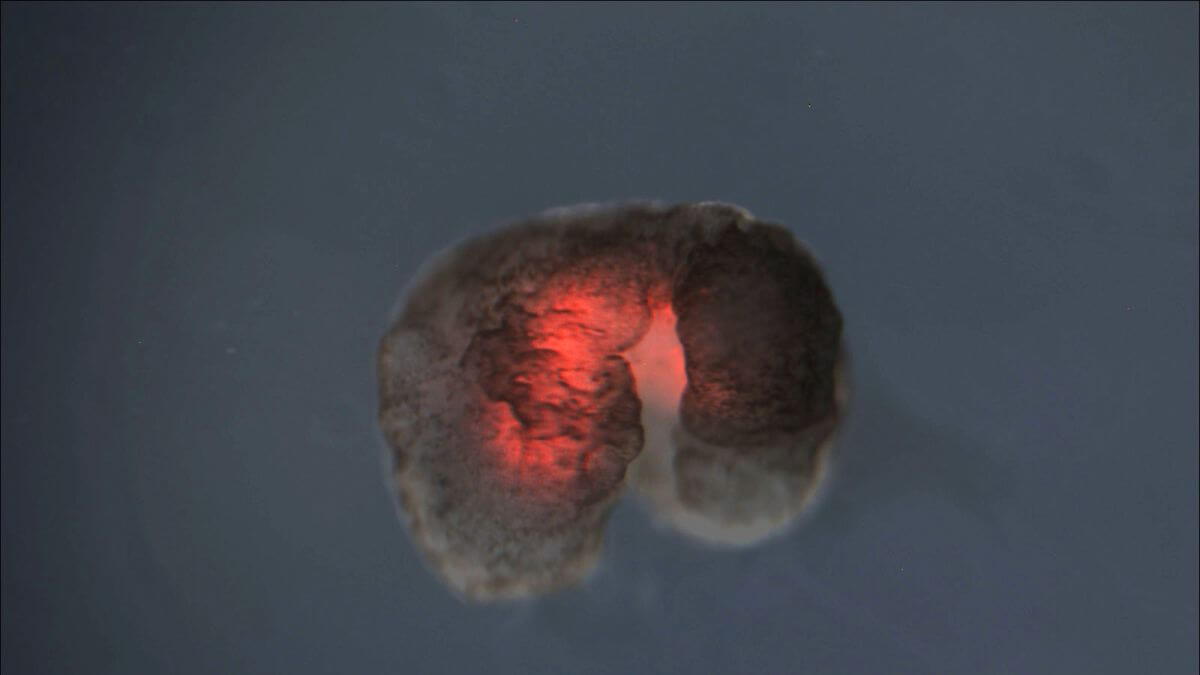
Um xenobot. Foto: Douglas Blackiston
As novas criaturas foram projetadas por um “algoritmo evolutivo” que roda em um supercomputador na UVM – e depois montadas e testadas por biólogos da Universidade Tufts. O programa começa gerando configurações aleatórias em 3D, de 500 a 1.000 células da pele e do coração. Cada projeto é então testado em um ambiente virtual, para ver, por exemplo, quão distante consegue se mover quando as células cardíacas são ativadas. Os projetos com melhor desempenho são usados para gerar mais designs, os quais são colocados em prática.
“Podemos imaginar muitas aplicações úteis desses robôs vivos que outras máquinas não podem fazer”, prevê Michael Levin, também co-líder da pesquisa e que dirige o Centro de Biologia Regenerativa e Desenvolvimento da Tufts, “como por exemplo rastrear uma contaminação radioativa, coletar microplásticos nos oceanos, ou viajar pelas artérias para remover placas de gordura.”
Os resultados da nova pesquisa foram publicados ontem nos Proceedings of the National Academy of Sciences.
Sistemas vivos criados sob medida
Embora a edição genética esteja avançando e já tenha criado organismos artificiais – copiando formas corporais de animais conhecidos – esta pesquisa, pela primeira vez na história, “projeta, desde o começo, máquinas completamente biológicas”, escreveu a equipe em seu novo estudo.
Com meses de processamento nos supercomputadores Deep Green no Vermont Advanced Computing Core da UVM, a equipe – a qual também faz parte Sam Kriegman, autor principal e doutorando – usou um algoritmo evolutivo para criar milhares de projetos candidatos para as novas formas de vida. Tentando realizar a tarefa que lhe foi atribuída pelos cientistas – como a locomoção em uma determinada direção –, o computador remontou várias vezes as células simuladas em inúmeras formas corporais. À medida que os programas eram executados – guiados por regras básicas sobre a biofísica do que a pele e as células cardíacas de um sapo podem fazer – os organismos simulados com maior sucesso foram mantidos e refinados, enquanto os projetos fracassados foram sendo descartados. Após cem execuções do algoritmo, os projetos mais promissores foram selecionados para teste.
A equipe da Tufts, liderada por Levin e com trabalho importante do microcirurgião Douglas Blackiston – deu vida aos projetos [promissores] in silico. Primeiro eles reuniram células-tronco, colhidas dos embriões de sapos africanos, espécie Xenopus laevis (daí o nome “xenobots”.) Estes foram separados em células únicas e deixados incubando. Depois disso, usando uma minúscula pinça e um eletrodo ainda menor, as células foram cortadas e unidas, para aproximarem-se dos projetos especificados pelo computador.
Reunidas em formas corporais nunca vistas na natureza, as células começaram a trabalhar juntas. As células da pele formaram uma arquitetura mais passiva, enquanto as contrações outrora aleatórias das células do músculo cardíaco foram colocadas em prática, criando movimentos ordenados pra frente, guiados pelo design do computador, e auxiliados por padrões espontâneos de auto-organização – permitindo que os robôs se movessem por vontade própria.
O estudo demonstrou que esses organismos reconfiguráveis são capazes de se mover de maneira coerente – e explorar o ambiente aquoso por dias ou semanas, alimentados por reservas embrionárias de energia.
Testes posteriores mostraram que grupos de xenobots conseguiram se movimentar em círculos e empurrar algo para um local central – de forma espontânea e coletiva. Outros foram construídos com um orifício no centro para reduzir o atrito no movimento. Nas versões simuladas, os cientistas conseguiram com sucesso redirecionar esse buraco como uma bolsa para transportar um objeto. “É um passo em direção ao uso de organismos projetados por computador para a entrega inteligente de medicamentos”, comemorou Bongard, professor do Departamento de Ciência da Computação e Centro de Sistemas Complexos da UVM.
Tecnologias vivas
Muitas dos dispositivos tecnológicos que conhecemos são feitos de aço ou plástico. Isso os tornam fortes ou flexíveis, mas podem gerar problemas para a saúde humana e problemas ecológicos, como a crescente poluição plástica nos oceanos e a toxicidade de muitos materiais sintéticos e eletrônicos. “A desvantagem do tecido vivo é que ele é frágil e se degrada”, compara Bongard. “É por isso que usamos aço. Mas os organismos têm 4,5 bilhões de anos de prática em se regenerar e continuar isso por décadas. E quando eles param de trabalhar – a morte – geralmente se desfazem inofensivamente. Esses xenobots são totalmente biodegradáveis. Quando terminam o trabalho após sete dias, são apenas células mortas da pele”.
Um laptop por exemplo, é uma tecnologia poderosa. Mas tente cortá-lo ao meio. Não funcionará mais. Nas novas experiências, os cientistas cortaram os xenobots e observaram o que aconteceu. “Cortamos o robô quase pela metade e ele se autocostura e continua”, diz Bongard. “E isso é algo que você não pode fazer com as máquinas tradicionais.”
Quebrando o código
Tanto Levin quanto Bongard consideram que o que estão aprendendo sobre como as células se comunicam e se conectam se estende profundamente à ciência computacional e à nossa compreensão da vida. “A grande questão da biologia é entender os algoritmos que determinam a forma e a função”, diz Levin. “O genoma codifica proteínas, mas aplicações transformadoras aguardam nossa descoberta de como esse hardware permite que as células cooperem para criar anatomias funcionais sob condições muito diversas”.
Time-lapse das células que estão sendo manipuladas e montadas, usando projetos in silico para criar os xenobots. Crédito: Douglas Blackiston, Universidade Tufts.
Para que um organismo se desenvolva e funcione, há muito compartilhamento e cooperação de informações – computação orgânica – acontecendo o tempo todo dentro e entre as células, não apenas dentro dos neurônios. Essas propriedades geométricas e emergentes são moldadas por processos bioelétricos, bioquímicos e biomecânicos, “que rodam em hardware especificado por DNA”, explicou Levin, “e esses processos são reconfiguráveis, possibilitando novas formas de vida”.
Os cientistas veem o trabalho “A scalable pipeline for designing reconfigurable organisms” – apresentado no PNAS – como um passo para a aplicação de insights sobre esse código bioelétrico à biologia e à ciência da computação. “O que realmente determina a anatomia em relação à qual as células cooperam?” Levin pergunta. “Você olha para as células em que construímos nossos xenobots e, genomicamente, são sapos. É 100% DNA de sapo – mas não são sapos. Então você pergunta, bem, o que mais essas células são capazes de construir?”
“Como mostramos, essas células de sapo podem ser persuadidas a criar formas vivas interessantes que são completamente diferentes da anatomia padrão”, extrapola Levin. Ele e os outros cientistas da equipe UVM e Tufts – com o apoio do programa Lifelong Learning Machines da DARPA e da National Science Foundation – acreditam que a construção dos xenobots é um pequeno passo para quebrar o que chamam de “código morfogenético”, que dá uma visão mais profunda da maneira geral como os organismos são organizados – e como eles calculam e armazenam informações com base em suas histórias e no ambiente.
Ameaça?
É natural que as pessoas se preocupem com as implicações das rápidas mudanças tecnológicas e dessas complexas manipulações biológicas. “Esse medo não é irracional”, compreende Levin. “Quando começarmos a mexer com sistemas complexos que não entendemos, teremos consequências não intencionais”. Muitos sistemas complexos, como uma colônia de formigas, começam com uma unidade simples – uma formiga – a partir da qual seria impossível prever o formato de sua colônia ou como eles podem construir pontes sobre a água apenas com seus corpos interligados.
“Se a humanidade sobreviver no futuro, precisamos entender melhor como propriedades complexas emergem de regras simples”, defende Levin. “Eu acho que é uma necessidade absoluta para a sociedade, que no futuro, tenha uma melhor noção de sistemas onde o resultado pode ser muito complexo. Um primeiro passo para fazer isso é explorar: como os sistemas vivos decidem qual deve ser um comportamento geral e como podemos manipular as peças para conseguir os comportamentos que queremos?
Em outras palavras, este estudo pode ser uma contribuição para entender do que as pessoas têm medo.
Imagem da capa: Joshua Bongard, University of Vermont.




L O U C U R A!!!!
Muito intedessa
Nte